전자빔 처리를 통한 발수성 금속 스텐트 제작 및 평가
This is an Open Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License(https://creativecommons.org/licenses/by-nc/3.0/) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
The objective of this study was to fabricate a novel hydrophobic stent for reducing restenosis by employing electron beam equipment. The stent was fabricated from a CoCr alloy tube by using a femtosecond laser and was treated with argon plasma. Subsequently, the stent’s surface specification changed from hydrophilic to hydrophobic. Application of the electron beam offers several advantages such as a short processing time, whole surface reforming, and enhancement of material properties. As the surface of the stent was rendered hydrophobic, it can provide equivalent or enhanced mechanical properties and greater functionality with a higher radial force at the extended stent in a blood vessel. The obtained results corresponding to the mechanical properties indicate that the contact angle increased to approximately 130o, and the radial force increased to approximately 3 N. Furthermore, cell culture experiments were conducted for verifying whether cells were cultured on the surface-modified CoCr surface. Based on the obtained results, it is believed that an effective reduction in the restenosis of inserted vascular stents is possible.
Keywords:
Stent, Electron beam treatment, Hydrophobic surface1. 서 론
심혈관 질환 중 하나인 심근경색은 혈관벽 내부에 콜레스테롤 등이 쌓여 혈관이 좁아지는 전신성 질환이다. 대표적인 치료 방법은 스텐트 시술기법으로, 튜브형태의 CoCr(Cobalt-Chromium)을 레이저 가공을 통해 미세 철망구조를 형성하고 혈관내 삽입하여, 좁아진 혈관을 물리적으로 확장시키는 기법이다. 이러한 외과적 시술 방법은 좁아진 혈관을 팽창시키는데 매우 효과적이며, 혈관 우회술과 같은 방법에 비해 비교적 간단한 수술기법으로 치료가 가능하다. 하지만, 스텐트 삽입 시술 이후 3-6 개월 이내에 병변 부분에 재협착(Restonosis) 증세가 발생하여 혈관벽이 다시 좁아지는 현상이 발생한다 [1]. 이러한 문제로 인해 스텐트 시술 후 정기적인 검진 및 주기적인 혈전 용해제와 같은 약물복용이 필수적으로 요구된다. 사용되는 약물은 주로 혈소판 생성 억제제와 같은 약물이며, 정기적인 약물 복용은 약물에 대한 내성 및 예상치 못한 사고 등의 문제로 인한 긴급 수술 등의 위험성을 내포한다. 이러한 문제를 극복하기 위해 약물 코팅 스텐트(Drug eluting stent) 등이 개발되어 스텐트 표면에 약물을 코팅하여 국부적인 약물 치료를 목표로 하였지만, 코팅된 약물의 담지량이 작아 스텐트 삽입 2-3주 후 코팅약물이 소모되기 때문에 이후 약물을 복용해야 하는 단점을 가진다 [2,3]. 이를 극복하기 위한 기법으로 펩타이드 및 해파린 등의 물질을 부착한 스텐트가 연구되고 있지만, 다양한 환경에서의 임상 실험 등의 난관이 있어 상용화에 어려움이 있으며, 공정의 복잡성 및 스텐트의 보관 방법 등의 문제를 내포하고 있다.
최근 약물 중심의 재협착 해결방법 대신에 금속 스텐트 표면 개질을 통해 재협착을 최소화하는 연구가 진행되었다 [4-6]. 이러한 방법은 혈관내 존재하는 단백질 기반의 혈장이 스탠트 표면에 흡착 정도를 최소화하여 재협착을 줄일 수 있 수 있다는 연구가 보고 되었다. 펨토초(Femtosecond) 레이저를 이용하여 스텐트 스트럿(strut) 표면 조도를 변경하고, 약물을 코팅 하여 재협착을 최소화하는 연구를 진행하였다 [4]. 이는 레이저를 이용하여 표면을 재 가공하기 때문에, 공정의 복잡성 및 스텐트 비용 상승이라는 문제를 가지고 있다. 또한, 금속 스텐트 표면에 질소 이온주입을 통해 표면 에너지를 변화시켜 재협착을 낮추는 연구를 진행하였지만 [6], 낮은 발수 특성 및 이온주입된 재료의 생체 적합성 여부 등의 생체 적합성 여부 판단이라는 문제를 내포하고 있다.
본 연구에서는 전자빔(Electron beam)을 이용하여 금속 스텐트 표면조도 및 에너지를 변화시키는 연구를 수행하였다. 대면적 전자빔을 이용한 표면처리는 공정이 매우 단순하고, 짧은 공정시간이내에도 효과적인 표면 개질이 가능한 장점을 가지며, 높은 발수 특성을 장기간 가져갈 수 있는 장점을 가진다. 이러한 공정 기법을 이용하여 CoCr 기반의 금속 스텐트를 산소(O) 분위기의 플라즈마에서 표면처리를 진행하고, 이에 따른 스텐트의 표면 분석 및 접촉각 분석을 진행하였다.
2. 연구 방법
2.1 금속 스텐트 표면 처리
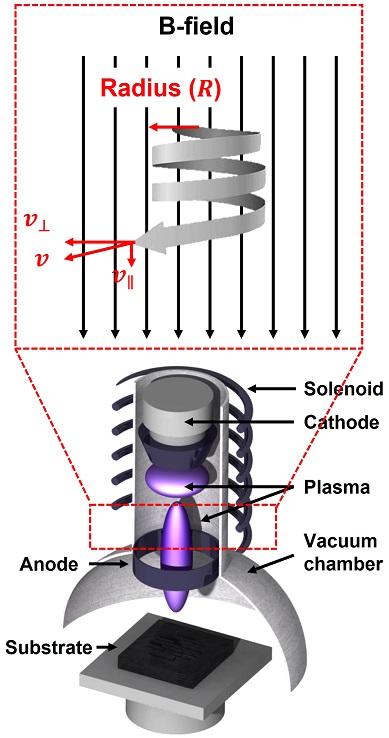
금속 스텐트는 펨토초 레이저를 이용하여 가공되었으며, 상용 제품과 동일한 생체적합성을 만족하는 CoCr 기반의 튜브로 가공되었다. 제작된 스텐트 스트럿의 크기는 약 100 μm의 두께를 가지며, 전남대학교병원 심혈관계 융합연구센터에서 제공되었다. 금속 스텐트는 산소 분위기의 반응 챔버에서 처리되었으며, 전자빔 표면처리 장치의 간략한 구조는 Fig. 1과 같다. 본 연구에서 수행한 스텐트는 0.05 Pa, 산소 분위기에서 30 keV의 에너지를 활용해, 3회 조사를 진행하였다.
전자빔 처리는 진공 분위기에서 반응성 가스를 이용하여 시료 전체에 표면 개질이 진행되기 때문에 복잡한 3차원 형태를 가지는 스텐트의 표면처리에 적합하다. 또한, 짧은 공정시간(-수 마이크로초) 및 여러 개의 스텐트 샘플을 일괄 처리할 수 있기 때문에 스텐트 대량생산에 매우 적합한 특징을 가진다. 이렇게 처리된 금속 스텐트는 친수성 특성에서 발수성 특성을 가지도록 표면이 개질 된다. 특히, 의료용으로 사용되는 재료의 경우 불순물의 유무에 따라서 사용 승인을 위한 임상실험 데이터가 요구되기 때문에, 재료 본연의 성분 외에 다른 재료가 혼합이 되지 않는 것이 상용화 측면에 유리하며, 임상시험에서 발생될 수 있는 부작용 등을 최소화할 수 있다. 전자빔 처리는 전계 방출로 방생되는 전자빔을 이용한 재료의 재결정화가 주를 이루며, 이로 인해 재료의 표면 조도 변화 및 표면 개질 층을 효과적으로 형성할 수 있어 재료 특성을 개선할 수 있는 장점을 가진다.
이러한 기법으로 표면 개질 된 스텐트를 XPS(X-ray photoelectron spectroscopy) 및 접촉각 측정 등을 진행하였다.
3. 결과 및 고찰
3.1 접촉각 분석
본 논문에서 제작된 스텐트는 Fig. 2(a)-(c)에 나타내었다. 스텐트 길이는 약 15 mm이며, 팽창 전 [Fig 2. (a)] 1 mm, 팽창 후[Fig. 2(c)] 약 3 mm 정도의 직경을 가진다. 일반 적인 금속 스텐트는 전기화학적 방법을 이용하여 CoCr 환봉을 스텐트 형상으로 레이저를 이용하여 가공하고, 전기-화학적 폴리싱을 수행하여 방법으로 표면 조도를 낮춘다. 이에 따른 SEM(Scanning electron microscope) 이미지는 Fig. 2(d)와 같으며, 발수성 특징을 부여하기 위해 전자빔 처리된 스텐트 SEM 이미지를 Fig. 2(e)에 나타내었다. 처리 전과 후의 SEM 이미지에서는 물리적인 표면 거칠기 변화는 관찰되지 않았다. 이는 표면 거칠기 변화에 따른 발수성 특성 변화가 아니며, 전자빔을 통한 CoCr 합금의 물성 변화라는 것을 3.2절의 XPS에서 확인할 수 있었다.
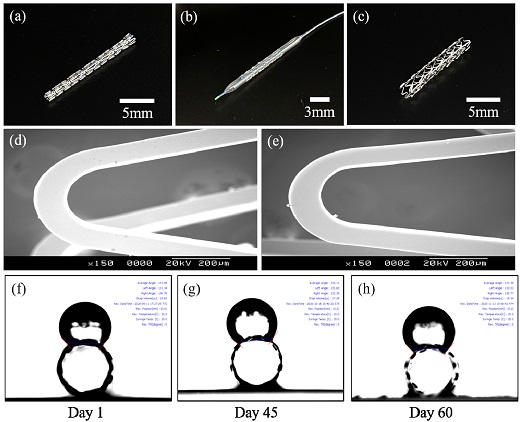
Photograph of the electron beam treated stent. (a) before expansion stent, (b) and (c) the extended stent by using balloon catheter, (d) and (e) the SEM photograph non-treated and treated stent respectively, (f) - (h) water contact results of the treated stent in during 2 months.
표면 개질 된 금속 스텐트의 발수 특징 분석을 접촉각 측정기를 이용하여 평가하였다. 일반적인 금속은 친수성 특성을 보이며, 이러한 특징은 스텐트가 혈관내 삽입되었을 때 혈장, 콜레스테롤 등이 쉽게 붙게 되어 재협착이 쉽게 발생된다. Fig. 2(e)−(h)와 같이 금속 스텐트의 발수성 특성을 분석하였으며, 측정 결과 약 129−131도의 높은 발수 특징을 가지는 것을 확인하였다. 일반적으로 재협착은 스텐트 시술 이후 2−3개월 동안 집중적으로 발생된다고 보고 되었으며, 이에 따라서 본 연구에서 개발한 금속 스텐트 또한 2개월에 걸친 발수성 테스트를 지속적으로 모니터링 하였다. 이에 따른 결과를 Table 1에 나타내었으며, 장기간 모니터링에서도 높은 발수각을 유지하는 것을 확인하였다.
일반적으로 레이저를 기반으로 한 스텐트 발수성 연구의 경우 레이저 빔의 조사 범위의 한계로 한쪽 면에 집중적으로 공정이 진행된다. 이는 스텐트 외부 및 내부 등 전체 면적에서 발생되는 재협작을 효과적으로 줄일 수 없는 단점을 가진다. 하지만, 본 연구에서 사용한 전자빔 처리 기법은 진공 챔버 내의 전체 공간에서 표면 개질이 이루어 지기 때문에 스텐트 스트럿의 전 면적에 걸쳐 공정이 진행된다. 이는 혈관에 삽입된 이후 환부에 접촉되는 물질의 접촉을 효과적으로 최소화할 수 있을 것으로 사료된다.
3.2 XPS 분석
Fig. 3은 전자빔 표면처리 적용 전/후 CoCr alloy 표면의 XPS 분석 결과를 보여준다. XPS 분석은 공기와 직접 접촉을 통해 형성하는 표면에서의 결합구조와 소재 내부에서의 결합구조 변화를 모두 분석하기 위해 아르곤 에칭을 통한 표면 식각을 활용해 수행되었다. Cr을 포함하는 합금의 경우, 표면에서 크롬 산화물을 형성하여 표면에너지를 낮추고 화학적 안정성을 부여할 수 있기 때문에 표면에 형성된 산화물의 종류에 따라 표면에너지와 내화학성이 결정된다. Fig. 3(a)에서 볼 수 있듯이, 전자빔 표면처리 적용 전 샘플 표면 (Bare)의 경우, Cr2O3의 Cr 화합물이 주로 형성된 것을 확인할 수 있지만 높은 비율의 Cr(OH)3 구조가 형성되어 있는 것을 확인할 수 있다. 또한, CrO3 화합물 형태의 산화물도 일부 존재하는 것으로 분석되었다.
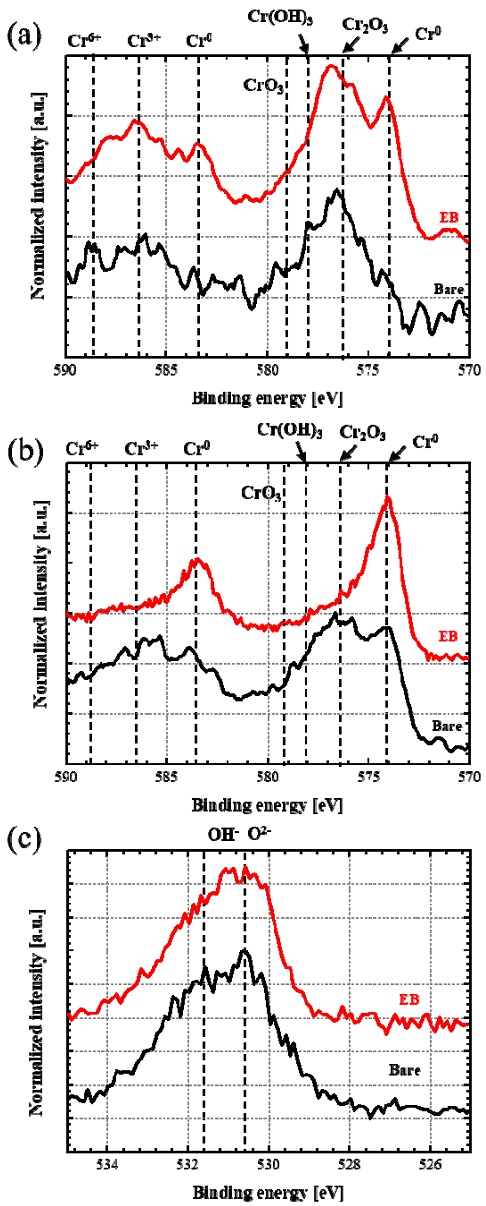
XPS results of the electron beam treated stent. (a) Cr-2p @ Top surface (0 s etching), (b) Cr-2p @ Sub-surface (1,000 s etching) and (c) O-1s results.
그러나, 전자빔 표면처리 (EB) 적용 후 표면에서 Cr이 대부분 Cr2O3의 형태로 존재하며, 높은 비중의 Cr metal 형태가 존재하는 것으로 나타났다. 이는 산소 가스를 활용한 전자빔 조사과정에서 플라즈마화 된 산소와 용융층이 높은 에너지로 인해 빠르고 안정적으로 Cr2O3를 형성한 것으로 분석할 수 있으며, 추가적인 산화반응 없이 나머지 Cr의 경우 순수 금속의 형태로 잔존하게 되는 것으로 분석할 수 있다 [7]. 또한 에칭 후 Sub-surface에서의 Cr-2p 그래프를 보면[Fig. 3(b)], 소재 내부에서 전자빔 표면처리에 의해 산화물이 거의 형성되지 않은 것을 확인할 수 있다. 전자빔 표면처리를 통해 형성되는 표면의 보호층은 소재 표면에서의 내화학성을 높여 산화, 부식 등의 화학적 반응으로 부터 소재를 보호하는 역할을 수행한다고 알려져 있다 [8]. 산소 가스를 활용한 본 연구에서의 전자빔 조사는 표면에서 기존의 아르곤 플라즈마 가스를 활용한 전자빔 조사에 비해 빠르고 안정적인 산화층 (Cr2O3)을 형성한 것으로 분석할 수 있으며, passivation layer의 역할을 효율적으로 수행하여 소재 내부에서 추가적인 산화가 발생하지 않도록 보호층의 역할을 수행한 것으로 판단된다.
전자빔 조사를 통한 표면에서의 결합구조 및 작용기 변화, 그리고 소재 내부에서의 산화 경향 변화는 표면에너지에 큰 영향을 미칠 수 있다. Fig. 3(a)에서 전자빔 조사 후 표면에서 –OH 작용기를 포함하는 결합의 비율이 감소하고 안정적인 구조를 가지는 Cr2O3가 형성된 것을 확인할 수 있고, 친수성 특성을 가지는 –OH 결합의 감소는 표면에너지 감소 및 접촉각 증가에 영향을 미치게 된다. 또한 소재 내부에서의 산화물 비율 감소 또한 표면에너지의 감소와 접촉각 증가 효과의 원인으로 분석할 수 있다.
이러한 경향은 XPS의 O-1s 그래프에도 잘 나타난다. Fig. 3(c)에서 볼 수 있듯이 O-1s 그래프에서도 전자빔 조사 후 상대적으로 OH-의 비율이 현저히 감소한 것으로 나타났으며, 이를 통해 전자빔 조사를 통한 표면에너지의 감소 및 접촉각 향상과 안정적인 산화층 형성을 통한 내화학성 부여가 가능함을 확인할 수 있다.
3.3 Radial force 평가
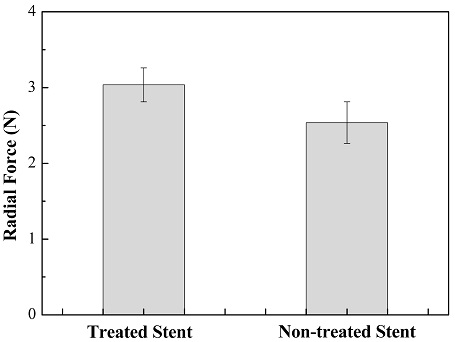
혈관내 삽입된 스텐트는 풍선 카테터를 이용하여 Fig. 2(b)-(c)와 같이 팽창된다. 팽창된 스텐트의 가장 중요한 평가 요소 중의 하나인 Radial force 측정은 팽창시킨 혈관 벽을 유지할 수 있는지를 평가하는 요소 중 하나이다. Radial force 평가는 전자빔 처리된 샘플 및 처리하지 않는 샘플의 두가지로 구분하여 평가하였으며 이에 따른 결과를 Fig. 4에 나타내었다. 먼저 전자빔이 처리되지 않은 샘플의 경우 최대 2.53±0.27 N의 값을 보이며, 전자빔 처리된 샘플은 최대 3.03±0.22 N의 값을 가지는 것으로 확인 되었다. 기본적으로 처리된 샘플 간의 극적인 차이는 발생하지 않았으며, 이는 테스트된 스텐트 스트럿의 디자인이 동일하기 때문이다. 전자빔 처리된 샘플이 약 0.5 N 정도 높은 이유는 이온빔 처리 동안 발생되는 표면 산화막 및 –OH의 감소, 그리고 표면 열처리에 의한 재료 표면 강도 변화에 따른 결과로 예측된다.
3.4 세포배양 테스트
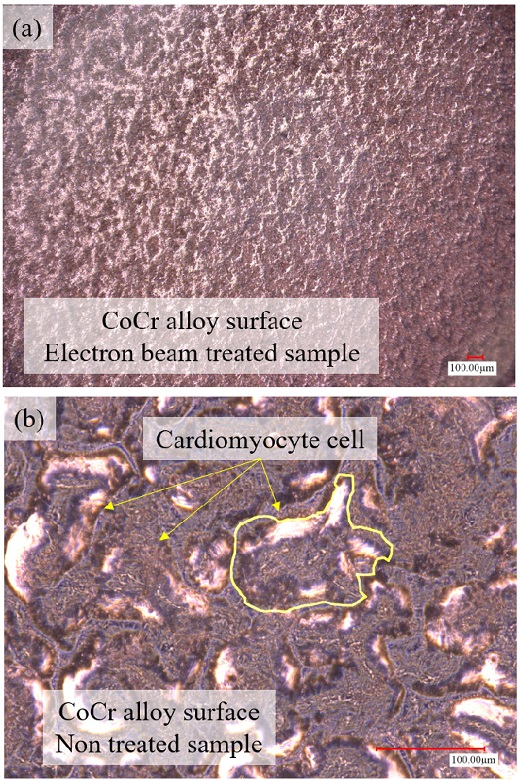
인체 삽입된 금속 스텐트는 혈관 내에서 혈전증을 발생시킬 수 있으며, 혈액과 생체 물질의 상호작용으로 스텐트 표면에 흡착되는 특징을 가진다. 피브리노겐(Fibrinogen), 본윌리브랜드 펙터(vWF, von willebrand factor), 알부민(Albumin) 및 파이브로넥틴(Fibronectin) 등과 같은 단백질은 혈액과 함께 스텐트 스트럿에 재협착을 촉진시키게 된다. 이러한 부착물에 의해 혈소판 유착이 발생되며 혈액응고 등과 같은 문제가 발생된다. 일반적인 금속 스텐트의 경우 FDA 승인된 생체적합성 물질을 사용하지만, 단백질의 쉬운 흡착으로 인해 혈관내부에서 재협착을 발생시키며, 항혈액응고 약물을 지속적으로 복용해야 하는 단점을 가진다. 전자빔 처리된 금속 스텐트의 경우 발수성 성질을 가지며, 1차적으로 단백질이 흡착이 어렵고, 이에 따른 신생내막 등과 같은 세포 성장이 어려워 재협착을 효과적으로 줄일 수 있다. 이러한 실험 결과는 Fig. 5와 같으며, 전자빔 처리된 CoCr 표면과 처리하지 않은 샘플의 경우 심장 근육 세포 성장이 안 되는 것을 실험을 통하여 확인하였고, 이는 재협착을 효과적으로 줄일 수 있을 것으로 사료된다.
4. 결 론
본 논문에서는 혈관 재협착을 줄이기 위해 제작된 스텐트의 표면처리를 수행하고 이에 따른 특성 평가를 진행하였다. 스텐트 표면처리는 이온빔 플라즈마를 이용하여 진행하였으며, 이에 따른 물리 화학적 분석을 XPS 등을 이용하여 분석하였으며, 기계적 특성의 변화 없이 표면처리에 따라 발수성질을 가지는 스텐트 개발을 완료하였다. 세포 배양 실험을 통해 표면 개질된 CoCr 표면에서의 세포 배양 여부를 확인 하였으며 이러한 결과를 기반으로 혈관 삽입된 스텐트의 효과적인 재협착 감소가 가능할 것으로 사료된다. 이로 인해 환자의 약물 복용을 최소화할 수 있으며, 이에 따른 약물 중독 및 약물 복용에 의한 환자의 비용감소 등과 같은 간접적 사회 비용을 줄일 수 있을 것으로 사료된다. 추후 연구로 표면 개질된 스텐트의 동물실험을 진행하여 실제 사용 가능여부 등을 파악할 예정이다.
Acknowledgments
본 연구는 한국연구재단 기본연구 지원 (2020R1F1A1074748, 2020R1F1A1071775)을 받아 수행 되었으며, 본 연구에 금속 스텐트 제작에 도움을 주신 전남대학교 의과대학 심혈관계융합센터 정명호 교수님과 연구팀, CG바이오에 감사의 말씀 올립니다.
REFERENCES
-
Levine, N. Glenn, P. Andrew, and L. Joseph, “Restenosis following coronary angioplasty: clinical presentations and therapeutic options”, Clin. Cardiol., Vol. 18, No. 12, pp. 693-703, 1995.
[https://doi.org/10.1002/clc.4960181203]

-
P. Vermeersch, P. Agostoni, S. Verheye, P. Van den Heuvel, C. Convens, F. Van den Branden, and G. Van Langenhove, “Increased late mortality after sirolimus-eluting stents versus bare-metal stents in diseased saphenous vein grafts: results from the randomized DELAYED RRISC Trial”, J. Am. Coll. Cardiol., Vol. 50, No. 3, pp. 261-267, 2007.
[https://doi.org/10.1016/j.jacc.2007.05.010]

-
S. Bangalore, B. Toklu, N. Amoroso, M. Fusaro, S. Kumar, E. L. Hannan, F. P. David, and F. Feit, “Bare metal stents, durable polymer drug eluting stents, and biodegradable polymer drug eluting stents for coronary artery disease: mixed treatment comparison meta-analysis”, Br. Med. J., Vol. 347, pp. f6625(1)-f6625(19), 2013.
[https://doi.org/10.1136/bmj.f6625]

-
I. H. Bae, M. H. Jeong, K. S. Lim, D. S. Park, J. W. Shim, J. K. Park, K. H. Oh, M. R. Jin, and D. S. Sim, “Novel Polymer-Free Everolimus Eluting Stent Fabricated using Femtosecond Laser Improves Re-endothelialization and Anti-infammatio”, Sci. Rep., Vol. 8, No. 1, pp.7383(1)-7383(11), 2018.
[https://doi.org/10.1038/s41598-018-25629-9]

-
I. H. Bae, M. H. Jeong, D. S. Park, K. S. Lim, J. W. Shim, M. K. Kim, and J. K. Park, “Mechanical and physio-biological properties of peptide-coated stent for reendothelialization”, Biomater. Res., Vol. 24, No. 1, pp. 4(1)-4(9), 2020.
[https://doi.org/10.1186/s40824-020-0182-x]

-
J. W. Shim, I. H. Bae, D. S. Park, K. S. Lim, S. Y. Lee, E. J. Jang, J. K. Park, J. H. Kim, and M. H. Jeong, “Evaluation of ion implantation for anti-thrombogenic coronary stent in vitro and in vivo”, J. Ind. Eng. Chem., Vol. 54, pp. 290-297, 2017.
[https://doi.org/10.1016/j.jiec.2017.06.003]

-
H. Luo, H. Su, G. Ying, C. Dong, and X. Li, “Effect of cold deformation on the electrochemical behaviour of 304L stainless steel in contaminated sulfuric acid environment”, Appl. Surf. Sci., Vol. 425, pp. 628-638, 2017.
[https://doi.org/10.1016/j.apsusc.2017.07.057]

-
J. Kim, S. S. Park, and H. W. Park, “Corrosion inhibition and surface hardening of KP1 and KP4 mold steels using pulsed electron beam treatment”, Corros. Sci., Vol. 89, pp. 179-188, 2014.
[https://doi.org/10.1016/j.corsci.2014.08.018]