ZnO 기반 NO2 가스센서의 MgZnO와 MgO을 통한 성능 향상에 대한 연구
This is an Open Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License(https://creativecommons.org/licenses/by-nc/3.0/) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
Brush-like ZnO hierarchical nanostructures decorated with MgxZn1-xO (x = 0.1, 0.2, 0.3, 0.4, and 0.5) were fabricated and examined for application to a gas sensor. They were synthesized using vapor phase growth (VPG) on indium tin oxide (ITO) substrates. To generate electronic accumulation at ZnO surface, MgZnO nanoparticles were prepared by sol-gel method, and the ratio of Mg and Zn was adjusted to optimize the device for NO2 gas detection. As the electrons in the accumulation layer generated by the heterojunction reacted faster and more frequently with the gas, the sensitivity and speed improved. When tested as sensing materials for gas sensors at 100 ppm NO2 at 300 oC, these MgZnO decorated ZnO nanostructures exhibited an improvement from 165 to 514 times compared to pristine ZnO. The response and recovery time of the MgZnO decorated ZnO samples were shorter than those of the pristine ZnO. Various analyzing techniques, including field-emission scanning electron microscopy (FESEM), energy-dispersive X-ray spectroscopy (EDS), and X-ray powder diffraction (XRD) were employed to confirm the growth morphology, atomic composition, and crystalline information of the samples, respectively.
Keywords:
Gas sensors, Oxide semiconductors, ZnO, NO2 gas1. 서 론
사물인터넷은 4차산업혁명의 주요 기술 중 하나로, 센서가 부착된 사물들이 네트워크를 통해 상호간의 정보를 생성, 수집, 공유 및 활용하는 기술이다[1]. 센서는 인간의 감각기관 역할을 하는 소자로 가스 센서, 이미지 센서, 습도 센서 등 사물에 오감을 부여한다[2]. 가스 센서는 유독성, 폭발성 가스를 감지하는 역할을 하며, 각종 유해로부터 인간이 안전한 생활환경을 영위할 수 있게 함은 물론 쾌적한 환경을 유지할 수 있게 한다[3,4].
가스센서는 작동 원리에 따라 전기화학식, 광학식, 산화물 반도체식, 접촉연소식 가스센서 등으로 분류된다[5]. 산화물 반도체식 가스센서는 타 방식과 비교하여 기존의 반도체 생산 공정과의 높은 호환성, 소형화, 낮은 제작단가 등의 장점으로 인하여, 다수의 연구가 이루어지고 있다[6-8]. 산화물 반도체는 주요 캐리어가 전자인지 정공인지에 따라 n-type과 p-type으로 구분된다. 전자를 주요 캐리어로 쓰는 n-type산화물 반도체는 정공을 사용하는 p-type 산화물 반도체에 비해 속도나 감도 면에서 뛰어나, n-type 산화물 반도체를 이용한 연구가 중심적으로 이루어지고 있다[9].
n-type 산화물 반도체의 경우, 산소 결핍의 비화학양론에 의해 200-400 oC 환경에서 표면에 대기 중의 산소가 흡착되고, 산소는 반도체로부터 표면 근처의 전자를 흡수하여 이온상태(O2-, O-, 또는 O2-)로 표면에 존재한다. 표면 인근의 산화물 반도체는 전자를 빼앗겨 고저항의 전자공핍층을 형성하고, 중심부는 반도성을 가져 전기적 core-shell 구조를 가진다[10, 11]. 산화성 가스는 산화물 반도체 표면 인근의 전자를 빼앗아 반도체 표면의 전자공핍층을 증가시킨다. 환원성 가스에 노출되면, 산화물 반도체의 흡착산소는 환원성 가스와 반응하여 반도체에게 전자를 돌려주고 동시에 표면에서 탈착된다. 이 과정에서 산화물 반도체의 저항이 감소한다[12].
ZnO는 독성 가스에 반응성이 높고, 제조단가가 낮으며, 높은 생체 적합성을 가져 가스센서에 많이 활용되는 대표적인 n-type 산화물 반도체이다[13].
가스센서는 감지하고자 하는 종류의 가스를 미량의 농도에서도 빠르게 감지할 수 있어야 한다. 따라서 선택성, 감도, 속도는 가스센서의 주요 파라미터이다[14]. 가스센서는 표면 반응을 하기 때문에 넓은 비표면적을 가지는 것이 중요하다. 입자가 작을수록 부피 대비 면적이 커지므로 가스 반응이 용이하나, 작아질수록 반데르발스 인력에 의해 나노입자가 뭉친 응집체가 형성될 가능성이 커진다. 응집체가 형성되면, 내부 입자가 외부로부터 차폐되어 가스와 반응하지 못하고, 이는 가스 감지 성능 악화로 이어진다[15, 16]. 높은 비표면적을 유지하기 위해서 많은 연구에서 수열합성법, 열수합성법, 기상증착법 등을 이용하여 높은 비표면적을 가지는 나노구조체를 성장시키고 있다[17-19]. 기상증착법은 고체 상태의 시료를 기화시켜 구조체를 형성시키는 방법으로, nm 단위의 구조체 제조가 가능하다[20].
가스센서는 가스의 종류에 따라 ppm에서 ppb 수준의 저농도 가스를 감지할 수 있어야 하므로, 나노구조체에 전이금속이나 다른 물질을 도핑하거나 장식하는 방법이 사용된다[21-23]. 그 중 sol-gel법은 산화물 반도체를 제조할 수 있는 기술로, 다성분계에서 전구체의 농도 및 조정이 용이하고 제조 단가가 저렴하고 제조 방법이 간단하다는 장점을 가진다[24].
본 논문에서는 ZnO 기반 가스센서의 성능 향상을 위해, ZnO를 나노구조체로 성장시키고 MgZnO와의 이종접합에서 전자축적층을 형성시켰다. 부산물로 발생하는 MgO와 ZnO 이종접합에 의한 공핍층의 영향을 고려하여, NO2가스에 대한 최적화를 연구하였다.
2. 연구 방법
2.1 나노브러쉬 ZnO 구조체 성장
Fig. 1(a)와 같이, 본 실험에서는 2 cm × 1 cm 크기의 유리를 기판으로 사용하였으며, 전극으로는 Indium Tin Oxide (ITO)를 사용하였다. 전극 사이 간격을 20μm으로 설정하기 위하여 레이저로 패턴을 식각 하였다. 기판은 Trichloroethylene, Acetone, Methanol, DI water 순서로 각 10분간 초음파 세정을 진행하였다.
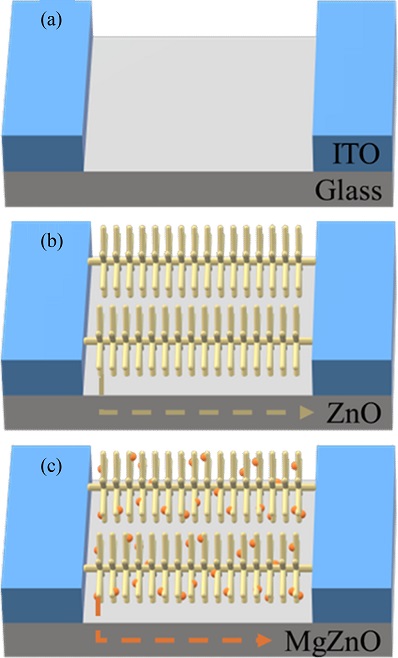
The Schematic of ZnO gas sensor decorated with MgZnO fabrication processes (a) the ITO substrate, (b) growing brush-like ZnO nanostructures, (c) decorating ZnO with MgZnO nanoparticles.
ZnO 나노구조체 성장을 위해, Zn (powder, <150 μm, 99.995%, Sigma-Aldrich Korea)를 알루미나 보트에 담아 퍼니스 중앙에 위치시켰다. 중앙으로부터 17~19 cm 떨어진 곳에 ITO 기판을 두었다. 증착 전, 쿼츠관 내부의 불순물을 제거하기 위해 로터리 펌프를 이용하여 30분간 저진공 상태를 유지하였다. 저진공 상태에서, 40분간 상온에서 900 oC까지 승온하였으며, 질량유량계(Mass Flow controller, MFC)를 이용하여 N2가스를 50 sccm 흘려주었다. 900 oC에 도달하였을 때, 1시간 동안 O2가스를 0.2 sccm 주입하며 ZnO 나노구조체를 성장시켰다(Fig. 1(b)). 공정이 끝난 후 급격한 온도 변화로 인한 나노구조체 붕괴 방지를 위해 상온까지 자연 냉각하였다.
2.2 MgZnO sol-gel 제조
Fig. 1(c)에서, 나노입자 형태로 MgZnO를 ZnO 나노구조체와 이종 접합을 형성하기 위하여, sol-gel 방식을 활용하였다. Magnesium acetate tetrahydrate(≥99%, Sigma-Aldrich Korea)와 Zinc acetate dihydrate(99.999%, Sigma-Aldrich Korea)를 전구체로 사용하였고, 용매로는 2-methoxyethanol(99.8%, Sigma-Aldrich Korea)을 사용하였다. 전구체가 용매에 잘 용해되도록 산성도를 조절하는 안정제로 ethanolamine(≥99.5%, Sigma-Aldrich Korea)를 사용하였다.
용액 농도는 0.1M로 설정하였고 Mg:Zn비율을 1:9부터 5:5까지 정수비로 설정하였다. 용액을 가열판 위에서 70 oC, 400 rpm 조건으로 2시간동안 교반한 뒤, 상온의 대기에서 하루동안 숙성하였다. Sol-gel 용액을 나노입자로 제조하기 위하여, 합성된 용액을 기판에 도포한 뒤 스핀 코팅 방법을 이용하여 3000 rpm 속도로 30초간 회전시키고 300 oC에서 10분 동안 가열판에서 용매를 날려주었다. 600 oC에서 퍼니스에서 대기압 환경에서 어닐링하여 나노입자를 제조하였다.
3. 결과 및 고찰
3.1 ZnO 나노브러쉬의 재료적 특성 분석
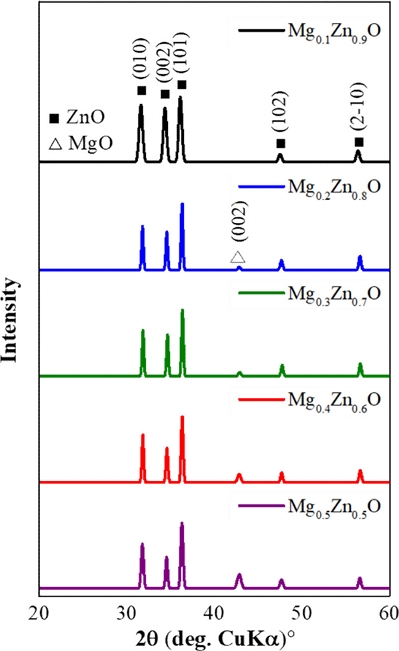
MgZnO의 결정 구조와 성분 분석을 위해 Fig. 2와 같이 XRD 분석을 하였다. 비율 별로 제조된 MgZnO 용액을 유리기판에 도포한 뒤 기존의 방식과 동일한 조건에서 어닐링하여 측정하였다. XRD 패턴에 대한 분석은 ICSD(Inorganic Crystal Structure Database)에 등록된 표준 값과 비교를 하였다. MgZnO는 ZnO구조에서 기존의 Zn 일부가 Mg로 대체된 물질로서, 치환된 Mg가 특정 비율 이하인 MgZnO는 ZnO의 구조가 유지되어 동일한 peak를 보인다[25]. 모든 MgZnO 시편은 ICSD:98-003-1052의 hexagonal ZnO peak와 일치함을 통해, Mg비율이 상승하여도 기본 ZnO의 wurtzite구조가 유지되었음을 확인하였다.
Mg의 비율이 20% 이상인 소자에서는 hexagonal ZnO외에도 ICSD:98-005-2026의 cubic MgO의 (002) peak가 추가로 검출되었고 Mg의 함량이 더 높은 소자일수록 더 높은 MgO peak를 나타나는 경향성을 보였다. Mg의 비율이 높을수록 ZnO구조에서 Zn를 치환하지 못하는 Mg의 양이 늘어나면서 MgO입자가 추가로 생성되었다. 이는 ZnO 표면에 MgZnO 나노입자 외에 MgO 나노입자도 함께 형성되었음을 의미한다.
제작된 ZnO의 나노구조체 형상과 MgZnO 나노입자를 확인하기 위해, 주사현미경(FE-SEM, field-emission scanning electron microscopy, SUPRA25, ZEISS, Germany)을 통해 분석하였다.
Fig. 3(a)를 통해, ITO 전극 사이의 간격이 20 μm이며, 나노 구조체가 기판 전반에 균일하게 성장하였음을 확인하였다. 전극 사이에 나노구조체가 성장함으로써 채널층 역할을 할 수 있음을 확인하였다.

FE-SEM images of (a) brush-like ZnO nanostructures growing evenly across the substrate, (b) brush-like ZnO networks, (c) details of nanostructures, (d) brush-like ZnO decorated with MgZnO nanoparticles.
높은 비표면적의 3차원 나노구조체는 하나의 기둥을 중심으로 다수의 와이어가 자란 브러쉬 형태로 성장했다(Fig. 3(b)). 중심기둥의 직경은 100-150 nm이며, 브러쉬를 구성하는 나노와이어의 직경은 20-50nm이고, 길이는 600-900 nm이다(Fig. 3(c)). 나노와이어 끝에 구 형태의 촉매 방울이 없는 것을 통해, ZnO가 기상증착법 중에서Vapor-Liquid-Solid가 아닌 Vapor-Solid 방식으로 성장하였음을 확인하였다.
Fig. 3(d)는 sol-gel을 통해, MgZnO 나노입자를 ZnO 나노구조체에 장식한 소자의 이미지이다. 공정 과정에서 ZnO 나노구조체가 붕괴되지 않고 브러쉬 형태를 유지하였으며, MgZnO나 노입자 간의 충분한 공간이 유지되어 응집체가 형성되지 않았음을 확인하였다.
MgZnO 나노입자가 도입된 브러쉬 형상의 ZnO 소자의 구성 원소를 분석하기 위하여 Fig. 4와 같이 Energy-Dispersive X-ray Spectroscopy (EDS, Ultim Max, Oxford Instruments, UK)를 사용하였다. Fig. 3과 마찬가지로 브러쉬 형상의 구조체가 확인되며(Fig. 4(a)), Fig. 4(b-d)에서 소자를 구성하고 있는 Mg, Zn, 그리고 O 성분을 확인할 수 있다. Mg은 MgZnO와 MgO의 구성 성분으로 ZnO 나노구조체를 이루는 Zn와 O에 비해 상대적으로 약한 강도로 검출되었다. Zn는 ZnO와 MgZnO의 구성성분이며, ZnO구조체로서의 비중이 더 높아, SEM 이미지의 구조체와 비슷한 형상으로 검출되었다. O는 모든 화합물에 포함되어 있어 전체적으로 고른 검출양을 보였다.
3.2 가스 반응 측정
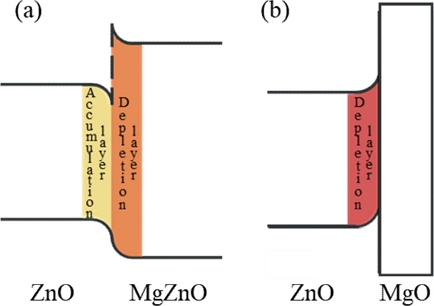
Fig. 5는 ZnO가 MgZnO 또는 MgO와 이종 접합을 형성하였을 때의 밴드 다이어그램을 나타낸다[26]. 가스와의 반응에 참여하는 중심 물질은 ZnO이므로, ZnO의 에너지 밴드 변화는 가스 감지 특성과 직결된다. ZnO와 MgZnO가 이종 접합을 형성하면, ZnO의 접합 계면에서는 전자축적층이 발생하여 저항이 감소하게 된다 (Fig. 5(a)). MgZnO에서 wurtzite 구조가 유지되는 비율(Mg ≤ 0.3, Mg+Zn=1)까지는 Mg 비율이 높아질수록 밴드갭이 넓어지며 접합 계면의 전자축적층에 더 많은 전자가 모인다[25]. 가스와의 반응에 참여가능한 전자 수의 증가는 NO2 가스에 대한 감도와 속도 향상으로 이어질 수 있다. Fig. 5(b)의ZnO와MgO의 접합 계면에서는 전자공핍층이 발생하기 때문에 오히려 반응에 참여가능한 전자의 수가 감소한다. 전자축적층을 통해 감도를 향상시키려는 방향과 반대의 현상이 나타나므로, MgO는 ZnO 가스센서의 성능을 저하시킨다. MgZnO sol-gel 용액 내의 Mg의 함량에 따라 MgZnO에 의해 유도된 전자 축적층과 MgO에 의한 공핍층의 비율이 달라지며, 가스 감지 성능이 달라진다.
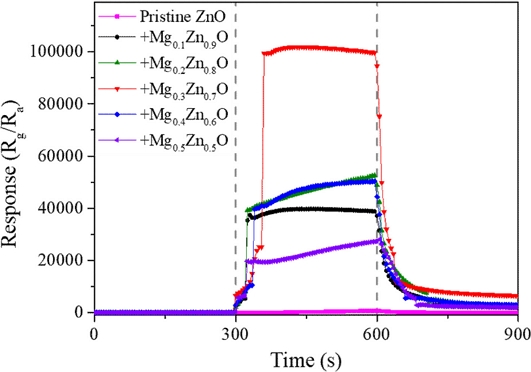
가스 센서 성능 비교 실험에서는 MgZnO 나노입자가 장식된 ZnO와 장식되지 않은 ZnO 소자의 가스 반응 특성을 비교하기 위하여, 300 oC 환경에서 100 ppm의 NO2 가스를 흘려주었다(Fig. 6). 안정화된 저항 Ra를 얻기 위해 저항이 안정화될 때까지 소자에 N2 가스를 흘려주었다. 300초 동안 안정화시킨 후 NO2 가스를 흘려주어 300초 동안 반응을 시켰으며, 다음 300초 동안 다시 N2 가스에서 회복시켰다.
소자가 반응 가스와 반응하기 전인 0~300초 사이의 평균 저항을 안정화 저항 Ra로 정의한다. 300초에서 600초 사이에는 가스센서를 NO2 가스에 노출시키고 이때, 변화하는 저항 값을 Rg라고 한다. 가스센서의 감도를 S = Rg/Ra로 정의하였다.
나노입자가 장식되지 않은 ZnO 소자의 감도는 166으로 가장 낮았다. Mg0.3Zn0.7O 소자의 반응성은 85242로 가장 높았으며, 순수 ZnO에 비해 514배 향상된 결과를 얻었다. Mg의 비율 30% 이하까지는 Mg의 비율이 증가함에 따라, 유도되는 전자축적층이 넓어져 감도가 높아지는 경향을 보였다. 하지만 30% 이후부터는 전자축적층이 넓어지지 않고 MgO에 의한 공핍층의 영향이 증가하여 반응성이 감소한다.
가스센서의 응답속도는 반응시간과 회복시간을 기준으로 한다. 본 논문에서는 최대 반응도의 90%까지 도달하는데 걸리는 시간을 반응시간으로, 최대 반응도의 10%까지 회복하는데 소요되는 시간을 회복시간으로 정의하였다.
Table 1에 순수 ZnO 가스센서와 농도별 MgZnO가 장식된 가스센서의 반응 시간과 회복 시간을 정리하였다. 순수 ZnO 가스센서의 반응 속도는 235초가 소요되었으며, 300초 이내에 회복하지 못하였다. Mg0.1Zn0.9O 소자는 순수 ZnO에 비해 반응 속도가 205초, 회복속도가 최소 225초의 값이 줄어들며, 가장 우수한 반응 속도를 보였다. XRD 분석에서 Mg0.1Zn0.9O 나노입자에서는 MgO이 검출되지 않았기 때문에, 해당 물질이 장식된 소자의 경우 MgO입자를 통해 생성된 공핍층의 영향이 가장 적으므로 가장 빠른 회복속도를 가진다. MgZnO가 장식된 가스센서 중 가장 느린 소자는 Mg0.5Zn0.5O 소자였으나 210초의 반응속도와 215 초의 회복 속도를 가져, 순수 ZnO에 비해 빠른 속도를 보였다.
선택성은 특정 가스의 종류와 농도를 가스를 구별해내는 능력으로, 가스 간의 감도비를 통해 나타낼 수 있다. 본 논문에서는 NO2 가스에 대한 감도를 NH3와 CO 가스에 대한 반응도로 나누어 NO2 가스에 대한 선택성을 분석하였다.
Table 2는 300 oC 환경에서 100 ppm 농도로, 동일한 조건 하에서 순수 ZnO소자와 MgZnO가 장식된 소자의 NO2, NH3, CO에 대한 가스에 반응도 및 선택성을 비교하였다. NH3와 CO는 환원성 가스이므로 반응도 S = Ra/Rg로 정의하였다. 순수 ZnO 소자가 NH3가스와 CO 가스에 노출되었을 때 각각1.1, 2.3의 반응도를 보여 NO2 가스에 대한 선택성을 72배, 151배의 선택성을 보였다. MgZnO가 장식된 ZnO는 모두 순수 ZnO에 비해 높은 선택성을 보였다. 가장 선택성이 높았던 소자는 Mg0.3Zn0.7O가 장식된 소자로, NH3, CO 가스 대비 25071배, 34097배의 선택성을 보였다.
4. 결 론
본 논문에서는 MgZnO 나노입자를 ZnO 나노구조체에 장식함으로써 감도, 속도 및 선택성이 향상된 산화물 반도체 가스센서를 제작하였다. 주사현미경 분석을 통해 ZnO가 나노브러쉬 형태의 구조체로 성장함을 확인하였다. 에너지분산형 분광분석법을 이용하여 기상증착법과 sol-gel 방식으로 제조한 물질의 성분을 분석하였다. X선 회절 분석을 통하여 MgZnO sol-gel 용액으로 제조한 산화물 반도체는 ZnO의 Hexagonal 구조를 가지고 있으며, Mg의 비율이 높은 용액에서는 MgO의 Cubic 구조도 함께 나타남을 확인하였다.
NO2 가스 반응 측정을 통해서 MgZnO 나노입자가 장식된 소자의 감도가 165배에서 514배까지 향상되었다. Mg0.3Zn0.7O소자까지는 Mg의 비율 증가에 비례하여 전자축적층이 늘어나 반응성이 향상되는 경향을 보였다. Mg의 비율이 높은 Mg0.5Zn0.5O와 Mg0.4Zn0.6O의 경우, MgO에 의한 공핍층의 영향이 증가하여 Mg0.3Zn0.7O가 장식된 소자에 비해 상대적으로 낮은 감도를 보였다. Mg0.1Zn0.9O 나노입자가 도포된 소자는 MgO 나노입자로 인한 공핍층의 영향을 받지 않아 가장 빠른 속도를 보였다. Mg0.3Zn0.7O가 장식된 ZnO 가스센서는 NO2의CO와 NH3에 대한 선택성은 25071배, 34097배로, 기존 소자에 비해 각 168배, 474배 향상된 결과를 보였다. MgZnO가 장식된 ZnO가스센서는 감도, 속도, 선택성에서 모두 순수 ZnO 소자 대비 우수한 성능을 보였다.
Acknowledgments
이 과제는 부산대학교 기본연구지원사업(2년)에 의하여 연구되었음.
REFERENCES
-
S. Munirathinam, “Chapter Six - Industry 4.0: Industrial Internet of Things (IIOT)”, Adv. Comput., Vol. 117, pp. 129-164, 2020.
[https://doi.org/10.1016/bs.adcom.2019.10.010]

-
I. H. Khan and M. Javaid, “Role of Internet of Things (IoT) in Adoption of Industry 4.0”, J. Ind. Integr. Manag., Vol. 6, No. 2, pp. 1-19, 2021.
[https://doi.org/10.1142/S2424862221500068]

-
A. Mirzaei, S. G. Leonardi, and G. Neri, “Detection of hazardous volatile organic compounds (VOCs) by metal oxide nanostructures-based gas sensors: A review”, Ceram. Int., Vol. 42, No. 14, pp. 15119-15141, 2016.
[https://doi.org/10.1016/j.ceramint.2016.06.145]

-
M. Kampa and E. Castanas, “Human health effects of air pollution”, Environ. Pollut., Vol. 151, No. 2, pp. 362-367, 2008.
[https://doi.org/10.1016/j.envpol.2007.06.012]

-
A. Dey, “Semiconductor metal oxide gas sensors: A review”, Mater. Sci. Eng. B-Adv. Funct. Solid-State Mater., Vol. 229, pp. 206-217, 2018.
[https://doi.org/10.1016/j.mseb.2017.12.036]

- N. Yamazoe, G. Sakai, and K. Shinmanoe, “Oxide semiconductor gas sensors”, Catal. Surv. Asia, Vol. 7, No. 1, pp. 63-75, 2003.
- Y. H. Kim, W. T. Koo, J. S. Jang, and I. D. Kim, “Review of Metal Oxide-based Formaldehyde Gas Sensor to Measure Indoor Air Quality”, J. Sens. Sci. Technol., Vol. 28, No. 6, pp. 377-384, 2019.
-
S. Yang, G. Lei, H. Xu, Z. Lan, Z. Wang, and H. Gu, “Metal Oxide Based Heterojunctions for Gas Sensors: A Review”, Nanomater., Vol. 11, No. 4, p. 1026, 2021.
[https://doi.org/10.3390/nano11041026]

-
G. Korotcenkov, V. Brinzari, I. A. Prionin, M. H. Ham, and B. K. Cho, “Metal Oxides for Application in Conductometric Gas Sensors: How to Choose?”, Solid State Phenomena, Vol. 266, pp. 187-195, 2017.
[https://doi.org/10.4028/www.scientific.net/SSP.266.187]

-
H. J. Kim and J. H. Lee, “Highly sensitive and selective gas sensors using p-type oxide semiconductors: Overview”, Sens. Actuator B-Chem., Vol. 192, pp. 607-627, 2014.
[https://doi.org/10.1016/j.snb.2013.11.005]

-
V. Kobrinsky, A. Rothschild, V. Lumelsky, Y. Komem, and Y. Lifshitz, “Tailoring the gas sensing properties of ZnO thin films through oxygen nonstoichiometry”, Appl. Phys. Lett., Vol. 93, No. 11, p. 113502, 2008.
[https://doi.org/10.1063/1.2982587]

-
D. R. Miller, S. A. Akbar, and P. A. Morris, “Nanoscale metal oxide-based heterojunctions for gas sensing: A review”, Sens. Actuator B-Chem., Vol. 204, pp. 250-272, 2014.
[https://doi.org/10.1016/j.snb.2014.07.074]

-
L. Wang, Y. Kang, X. Liu, S. Zhang, W. Huang, and S. Wang, “ZnO nanorod gas sensor for ethanol detection”, Sens. Actuator B-Chem., Vol. 162, No. 1, pp. 237-243, 2012.
[https://doi.org/10.1016/j.snb.2011.12.073]

-
N. Yamazoe, “Toward innovations of gas sensor technology”, Sens. Actuator B-Chem., Vol. 108, No. 1-2, pp. 2-14, 2005.
[https://doi.org/10.1016/j.snb.2004.12.075]

-
H. R. Kim, K. I. Choi, J. H. Lee, and S. A. Akbar, “Highly sensitive and ultra-fast responding gas sensors using self-assembled hierarchical SnO2 spheres”, Sens. Actuator B-Chem., Vol. 136, No. 1, pp. 138-143, 2009.
[https://doi.org/10.1016/j.snb.2008.11.016]

-
A. Z. Sadek, S. Choopun, W. Wlodarski, S. J. Ippolito, and K. Kalantar-zadeh, “Characterization of ZnO Nanobelt-Based Gas Sensor for H2, NO2, and Hydrocarbon Sensing”, IEEE Sens. J., Vol. 7, No. 6, pp. 919-924, 2007.
[https://doi.org/10.1109/JSEN.2007.895963]

-
G. Zhu, C. Xi, H. Xu, D. Zheng, Y. Liu, X. Xu, and X. Shen, “Hierarchical NiO hollow microspheres assembled from nanosheet-stacked nanoparticles and their application in a gas sensor”, RSC Adv., Vol. 2, No. 10, pp. 4236-4241, 2012.
[https://doi.org/10.1039/c2ra01307j]

- F. Liu, L. Li, F. Mo, J. Chen, S. Deng, and N. Xu, "A Catalyzed-Growth Route to Directly Form Micropatterned WO2 and WO3 Nanowire Arrays with Excellent Field Emission Behaviors at Low Temperature", Cryst. Growth Des., Vol. 12, No. 1, pp. 7-17, 2004.
-
R. L. V. Wal, G. M. Berger, M. J. Kuils, G. W. Hunter, J. C. Xu, and L. Evans “Synthesis Methods, Microscopy Characterization and Device Integration of Nanoscale Metal Oxide Semiconductors for Gas Sensing”, Sensors, Vol. 9, No. 10, pp. 7866-7902, 2009.
[https://doi.org/10.3390/s91007866]

-
D. Calestani, M. Zha, R. Mosca, A. Zappettini, M. C. Carotta, V. D. Natale, and L. Zanotti, “Growth of ZnO tetrapods for nanostructure-based gas”, Sens. Actuator B-Chem., Vol. 144, No. 2, pp. 472-478, 2010.
[https://doi.org/10.1016/j.snb.2009.11.009]

-
S. W. Choi, A. Katoch, G. J. Sun, J. H. Kim, S. H. Kim, and S. S. Kim, “Dual Functional Sensing Mechanism in SnO2–ZnO Core–Shell Nanowires”, ACS Appl. Mater. Interfaces, Vol. 6, pp. 8281-8287, 2014.
[https://doi.org/10.1021/am501107c]

-
V. Kumar, S. Sen, K. P. Muthe, N. K. Gaur, S. K. Gupta, and J. V. Yakhmi, “Copper doped SnO2 nanowires as highly sensitive H2S gas sensor”, Sens. Actuator B-Chem., Vol. 138, No. 2, pp. 587-590, 2009.
[https://doi.org/10.1016/j.snb.2009.02.053]

-
D. Zappa, V. Galstyan, N. Kaur, H. M. M. M. Arachchige, O. Sisman, and E. Comini, “Metal oxide -based heterostructures for gas sensors- A review”, Anal. Chim. Acta., Vol. 1039, pp. 1-23, 2018.
[https://doi.org/10.1016/j.aca.2018.09.020]

-
H. Dislich, “Sol-gel: Science, processes and products”, J. Non-Cryst. Solids, Vol. 80, No. 1-3, pp. 115-121, 1986.
[https://doi.org/10.1016/0022-3093(86)90384-4]

-
B. Sarikavak-Lisesivdin, “Numerical optimization of two-dimensional electron gas in Mgx Zn1−x O/ZnO heterostructures (0.10<x<0.30)”, Philos. Mag., Vol. 93, No. 9, pp. 1124-1131, 2013.
[https://doi.org/10.1080/14786435.2012.741728]

-
T. C. Zhang, Y. Guo, Z. X. Mei, C. Z. Gu, and X. L. Du, “Visible-blind ultraviolet photodetector based on double heterojunction of n-ZnO/insulator-MgO⁄p-Si”, Appl. Phys. Lett., Vol. 94, No. 11, p. 113508, 2009.
[https://doi.org/10.1063/1.3103272]