Polygalacturonase를 검출하기 위한 종이 기반의 효소결합 면역반응 센서 제작
This is an Open Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License(https://creativecommons.org/licenses/by-nc/3.0/) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
In this paper, we describe the fabrication of a paper-based enzyme-linked immunosorbent assay (ELISA) to detect polygalacturonase (PG), which is used as a biomarker to determine whether a plant is infected with a disease. The proposed paper-based ELISA can analyze the concentration of PG in a short time using a small sample compared to the traditional ELISA, which is generally performed using a well plate. To increase the resolution of the sensor, we optimized the dilution ratio of the HRP-conjugated goat anti-rabbit IgG antibody and the dilution ratio of the anti-PG and HRP-conjugated goat anti-rabbit IgG antibodies. Furthermore, for quantitative analysis of PG concentration, Delta RGB analysis was conducted to detect color changes in the sensing window displayed by the PG samples at various concentrations. Based on the experiment, the fabricated paper-based ELISA could measure at least 0.25 μg of PG and the measurement range was 0.25–2 μg. Therefore, the paper-based ELISA for detecting PG is expected to be able to determine the presence or absence of disease in crops at the infection stage in the future.
Keywords:
Polygalacturonase (PG), Enzyme-linked immunosorbent assay (ELISA), Paper-based ELISA1. 서 론
식물을 구성하는 식물세포는 일반적으로 펙틴(pectin), 헤미셀룰로오스(hemicellulose), 셀룰로오스(cellulose) 복합체로 이루어져 있으며 세포벽을 견고하게 하고 외부로부터 침입하는 병원체를 방어하는 물리적·화학적 장벽 역할을 한다 [1]. 식물은 일생 동안 다양한 병원균에 의해 영향을 받아 생장하는데 박테리아 및 진균 같은 병원균은 병원체가 식물세포 내로 침투할 수 있게 다양한 펙틴 분해 효소를 생성한다. 그 중에서 Polygalactronase(PG, EC 3.2.1.15)는 펙틴(Pectin) 분해 효소중 하나로 펙틴사슬 사이에 물 분자를 첨가해서 α-(1,4)-glycosidic bond를 끊고 펙틴을 분해하는 역할을 한다. 특히, 식물에서 PG는 질병감염의 초기와 숙주 정착(host colonization) 동안 많이 생성되며 조직 침범(tissue maceration)과 연성 부패(soft rot)를 특징으로 하는 식물 질병에 매우 관련성 많은 것으로 알려져 있다 [2,3]. 그러므로, 식물에서 PG의 유무는 식물 내로 병원체의 침입 여부를 확인할 수 있는 기준이 될 수 있으므로 PG의 유무를 검출하는 연구는 매우 중요하다.
대부분의 병을 일으키는 곰팡이는 식물의 세포벽을 분해하기 위해 다양한 효소를 생성하며 효소는 병원체가 식물 조직 내부의 침투 및 균사 분사 분지에 중요한 역할을 한다 [4-6]. 특히, 다양한 펙틴 분해 효소 중 하나인 PG는 곰팡이에 탄소원을 제공해 주는 펙틴을 분해하여 식물의 병원체 감염에 결정적인 역할을 하기 때문에 식물체 내에서 PG의 검출은 식물의 질병감염 여부를 판단하는데 있어 기준이 될 수 있으므로 매우 중요하다 [7,8].
기존의 PG의 검출 방법으로는3,5-dinitrosalicy acid(DNS) 방법, Somogyi-nelson 방법 및 Rythenium Red(RR) 방법 등이 있으며 위 방법들은 샘플에 있는 PG의 활성도에 따라 변화는 색의 변화를 스펙트로미터(spectom eter)를 활용한 흡광도 측정을 통해 PG의 활성도를 측정하였다 [9-12]. 하지만 기존의 분석 방법들은 샘플 내 PG의 활성을 측정할 수 있지만 PG의 양을 정량적으로 분석할 수 없으며 검출하는 과정이 복잡하고 고가의 장비인 스펙트로 미터가 필요하다는 단점을 가지고 있다. 최근에 현장에서는 신속하고 간단하게 생·화학적인 물질을 검출할 수 있는 센서에 대한 요구가 계속적으로 증가하고 있다. 그래서 저렴하면서 휴대가 용이하며 소량의 시약으로 빠른 분석을 제공할 수 있는 특징을 가진 종이기반 센서의 개발이 주목 받고 있으므로 샘플 내에 PG의 양을 검출하는 센서로도 활용을 고려할 수 있다.
본 연구에서는 샘플 내에 있는 PG를 정량적으로 분석할 수 있는 종이 기반의 효소결합 면역반응 센서의 제작 및 그 성능을 실험하였다. PG의 양을 검출하기 위한 종이 기반의 효소결합 면역반응 센서는 왁스프린팅 방법을 사용하여 쉽고 간단하게 제작되었으며 샘플 내 PG 양 측정은 센싱부의 색 변화를 Delta RGB 값을 분석하여 정량화 하였다. 특히, 제안된 센서는 약 3 μl의 소량 샘플을 사용하여 2시간 내에 샘플 내에 PG의 양을 정량적으로 분석할 수 있다는 장점을 가진다.
2. 연구 방법
2.1 종이 기반의 효소결합 면역반응 센서의 설계 및 제작
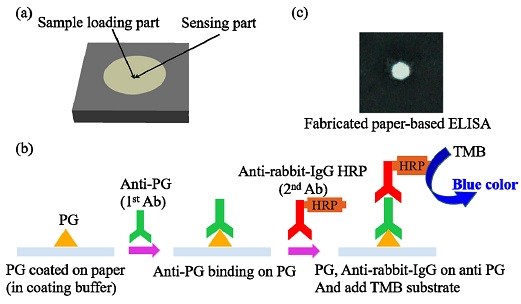
PG의 양을 측정하기 위해 제안된 센서는 단층으로 이루어졌으며 지름 4 mm 크기 원형 부분을 샘플 주입부 및 센싱부로 같이 사용한 구조로 설계되었다. Fig. 1(a)는 종이 기반의 효소결합 면역반응 센서의 개략도를 보여준다. 종이 기반의 효소결합 면역반응 센서는 먼저 센서의 구조 및 형상을 AutoCAD를 사용하여 설계한 후 설계된 센서를 왁스프린터를 사용하여 종이 위에 왁스를 프린팅 한다. 다음으로 종이 표면 위에 있는 왁스를 종이 내부로 완전히 침투 시키기 위해 왁스가 패턴된 종이를 평판가열기(hotplate) 위에 놓고 120oC에서 3분 동안 가열하면 센서의 제작이 완료된다. Fig. 1(c)는 왁스프린터를 사용하여 제작된 종기 기반의 효소결합 면역반응 센서의 광학적 이미지를 보여준다.
2.2 종이 기반의 효소결합 면역반응 센서의 구동 원리
종이 기반의 효소결합 면역반응 센서의 구동 원리는 다음과 같다. 왁스프리팅 방법을 사용하여 제작된 종이센서의 샘플 주입부 영역에 phosphate buffer saline(PBS) 용액을 사용한 희석한 샘플을 3 μl 넣고 20분 정도 샘플을 배양한다. 샘플 배양 후 washing buffer로 세척한 다음 2 % bovine serum albumin(BSA)가 포함되어 있는 blocking buffer를 3 μl 첨가하고 10분 동안 반응시킨 후 washing buffer를 사용하여 다시 세척한다. 다음으로, blocking buffer에 희석된 anti-PG 항체를 3 μl 첨가한 후 다시 20분 동안 반응하도록 두었다가 washing buffer로 씻어낸다. 마지막으로 goat anti-rabbit horseradish peroxidase(HRP) 항체를 3 μl 첨가한 후 다시 10분 동안 반응하도록 두었다가 washing buffer로 다시 씻어준다. 종이가 건조되면 3 μl의 tetramethylbenzidine(TMB) substrate solution를 센싱부에 넣은 후 30분 방치하고 센싱부의 색의 변화를 확인하여 샘플내 PG의 양을 정량화 할 수 있다. Fig. 1(b)는 종이 기반의 효소결합 면역반응 센서의 구동 원리를 보여준다. 만약, 샘플 내에 PG가 있다면 센싱부의 색이 흰색에서 파란색으로 발색되며 PG의 양이 많을수록 더욱 진한 파란색으로 발색되므로 발색되는 정도를 Delta RGB 값 분석을 통해 PG의 양을 정략적으로 분석할 수 있다.
2.3 시약 및 기구
PG를 정량적으로 측정하기 위한 센서를 제작하기 위해 다양한 시약이 사용되었다. 센서의 플랫폼으로 사용되는 Whatman Grade 1 CHR chromatography paper는 GE healthcare제품을 사용하였다. PG는 Novozymes에서 구매하였고, goat anti-rabbit IgG HRP는 Cell signal 제품을 사용하였다. 기본 완충액으로 사용된 PBS, washing solution으로 사용된 Tween20, blocking solution으로 사용된 BSA은 Sigma 제품을 사용하였다. 접합된 HRP의 발색을 위해 사용된 TMB substrate solution은 Thermo 제품을 사용하였다.
PG 검출센서를 제작하기 위해 AutoCAD프로그램을 사용하여 센서의 형상 및 구조를 설계하였으며, Xerox ColorQube 8570DN 프린터를 사용하여 설계된 센서를 종이 위에 형상화 했다. 제안된 종이기반의 효소결합 면역반응 센서를 사용하여 PG의 양을 정량적으로 분석하기 위해 일정한 빛의 밝기가 유지되는 공간에서 센서의 센싱부 이미지를 Sony의 α-5100 디지털 카메라를 이용해서 획득했다. Fig. 2는 일정한 빛의 밝기가 유지된 PG 측정 시스템을 보여준다.
2.4 이미지 분석
디지털 카메라를 통해 획득한 종이 기반의 효소결합 면역반응 센서의 센싱부 이미지는 Image J 프로그램으로 분석하여 센싱부에 대한 평균 RGB값을 획득했다. Delta RGB 값은 PG가 존재하지 않는 샘플에서 얻어진 센싱부의 평균 RGB값(R0, G0, B0)과 PG가 존재하는 샘플에서 얻어진 센싱부의 평균 RGB값(Rn, Gn, Bn)의 차이를 이용하여 정량적으로 분석된다. 측정의 정확성을 위해 동일 샘플에 대한 Delta RGB 분석은 3번 반복을 통해 얻었다.
| (1) |
3. 결과 및 고찰
3.1 PG를 검출하기 위한 종이 기반 효소결합 면역반응 센서의 최적화
종이 기반 효소결합 면역반응 센서를 사용하여 PG를 검출하기 위해서는 센서의 최적화가 필요하며 이에 영향을 미치는 다양한 요소들을 고려하여 센서를 설계 및 제작했다. 제안한 센서는 항원과 항체의 면역반응을 HRP가 접합된 goat anti rabbit IgG항체와 TMB substrate 용액의 반응에 의해 나타나는 발색의 크기를 분석하여 PG의 양을 검출하는 것을 기본 원리로 함으로 TMB substrate 용액과 반응하는 goat anti rabbit IgG 항체의 희석 비율과 goat anti rabbit IgG 항체와 반응하는 anti-PG항체의 희석 비율이 센서의 분해능에 미치는 영향이 매우 크다. 그러므로 HRP가 접합된 goat anti rabbit IgG 항체의 희석 비율과 anti-PG항체의 희석 비율을 최적화 할 필요가 있다.
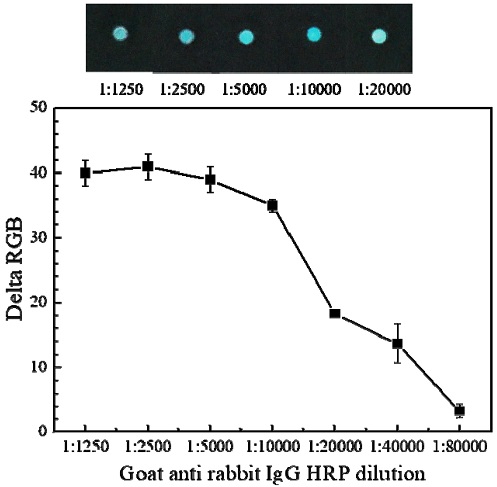
첫 번째로 HRP가 접합된 goat anti rabbit IgG 항체의 희석비율을 결정하기 위해서 다양한 농도로 희석된 goat anti rabbit IgG항체와 TMB substrate 용액을 반응시켜 발색의 크기를 비교 분석 하였다. 실험에 사용된 HRP가 접합된 goat anti rabbit IgG 항체의 희석 비율 범위는 1:1250부터 1:80000이다. Goat anti rabbit IgG항체의 희석 비율을 최적화하기 위한 실험은 먼저 HRP가 접합된 goat anti rabbit IgG 항체를 PBS 용액에 희석하여 종이센서 센싱부에 3 μl 주입하고 20분 동안 배양한 다음 TMB substrate 용액을 첨가하여 30분 동안 반응 후 발색의 정도를 비교분석 하였다. 실험결과 HRP가 접합된 goat anti rabbit IgG 항체의 희석 비율 1:1250부터 1:5000 사이에서 Delta RGB 값이 오차 범위 내로 가장 크게 나타나는 것을 알 수 있으며, 센서를 저가로 제작하기위해 최적의 희석 비율을 1:5000으로 결정하였다. Fig. 3은 goat anti rabbit IgG HRP 희석 비율에 따른 TMB 발색을 Delta RGB로 분석한 값을 보여준다.
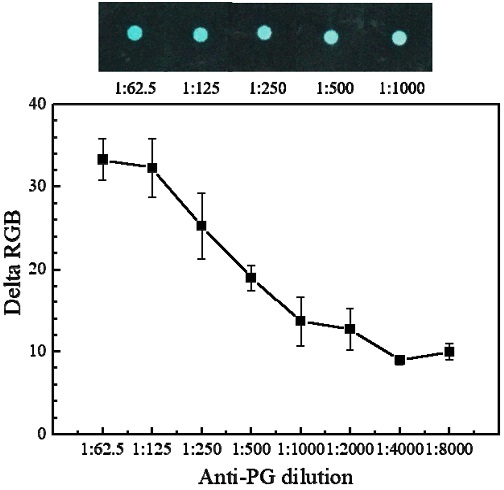
다음으로 anti-PG 항체의 희석 비율을 결정하기 위해 다양한 농도로 희석된 anti-PG 항체와 1:5000으로 희석된 HRP가 접합된 goat anti rabbit IgG 항체와 반응시켜 발색의 크기를 비교분석 하였다. 실험에 사용된 anti-PG 항체의 희석 비율 범위는 1:62.5부터 1:8000 이다. Anti-PG 항체의 희석 비율을 최적화하기 위한 실험은 먼저 anti-PG 항체를 PBS 용액에 희석하여 종이센서 센싱부에 3 μl 주입하고 20분 동안 배양한 다음 blocking 후 씻어내고 1:5000으로 희석된 HRP가 접합된 goat anti rabbit IgG 항체를 3μl 첨가하고 반응시킨다. 반응 후 마지막으로 3 μl TMB substrate 용액을 첨가하여 30분 동안 반응 시킨 다음 희석 비율에 따른 발색의 정도를 비교분석 하였다. 실험결과 anti-PG 항체의 희석 비율 1:62.5부터 1:125 사이에서 Delta RGB 값이 오차 범위 내로 가장 크게 나타나는 것을 알 수 있으며, 센서를 저가로 제작하기 위해 최적의 희석 비율을 1:125로 결정하였다. Fig. 4는 종이 센서에서 anti-PG와 goat anti rabbit IgG 항체 상호 반응에 따른 희석비율 최적화를 보여준다.
위의 실험결과들을 바탕으로 PG의 양을 고분해능으로 검출하기 위해서 종이 기반의 효소결합 면역반응 센서에 1:5000으로 희석된 HRP가 접합된 goat anti rabbtit IgG 항체와 1:125 로 희석된 anti-PG 항체를 사용하였다.
3.2 종이 기반의 효소결합 면역반응 센서를 사용한 PG 양의 정량적인 분석
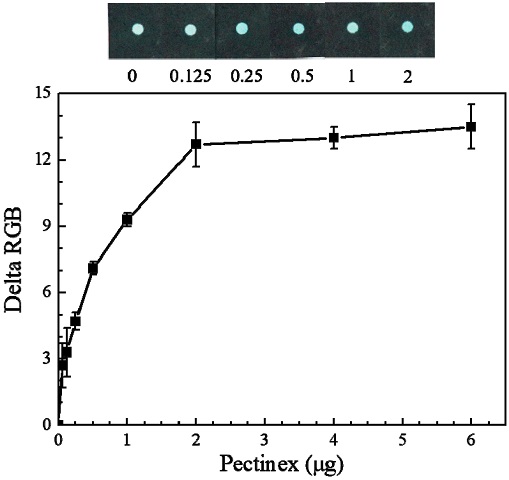
위의 실험결과들을 기반으로 최적화된 종이 기반의 효소결합 면역반응 센서를 제작하였으며 이를 사용하여 다양한 양을 가진 PG 샘플에 대해서 정량적으로 분석하였다. 실험에서 사용한 샘플의 PG의 양 범위는 0부터 4 μg 이며 PG의 양에 따른 센싱부의 Delta RGB 값을 분석하여 PG의 양을 정량화하기 위한 실험을 진행하였다. 실험은 제작된 종이센서 센싱부에 다양한 양을 가진 PG 샘플 3 μl 주입하고 20분 동안 배양한 다음 blocking 과정 및 씻어낸 후 1:125 비율로 희석된 anti-PG 항체와 1:5000 비율로 희석된 HRP가 접합된 goat anti rabbit IgG 항체를 3 μl를 순서대로 첨가하고 반응시켰다. 반응 후 마지막으로 TMB substrate 첨가하여 30분 동안 반응 시킨 후 발색의 정도를 비교 분석 하였다. 실험결과 종이센서를 사용하여 0 μg 부터 0.125 μg을 가진 PG 샘플을 분석한 결과 센싱부의 Delta RGB 변화가 거의 없었으며 0.25 μg 부터 유의미한 Delta RGB 값의 변화를 확인할 수 가 있었다. Fig. 5는 다양한 양의 PG를 가진 샘플에 따른 Delta RGB값의 변화를 보여준다. PG의 양이 0.25 μg일 때 센싱부의 Delta RGB 값은 4.7이며 PG의 양이 2 μg 일 때 센싱부의 Delta RGB 값은 12.7로 가장 큰 것을 알 수 있다. 2 μg 보다 많은 양의 PG 샘플에서는 항원-항체 반응이 포화되어 발색 크기가 변화가 거의 없는 것을 알 수 있다. 제안한 종이 기반의 효소결합 면역반응 센서로 검출한 가능한 PG의 양은 0.25 μg-2 μg 임을 알 수 있었다.
4. 결 론
본 논문에서는 식물의 질병 감염 여부를 판단하는 바이오 마커로 사용되는 PG를 검출하기 위한 종이 기반의 효소결합 면역반응 센서의 제작 및 제작된 센서의 성능에 대해서 평가하였다. 제안된 센서는 왁스프린팅방법을 사용하여 간단하게 제작하였으며 제작된 센서의 성능 평가는 다양한 농도를 가진 PG 샘플을 센싱부에 놓고 면역반응을 통해서 나타나는 센싱부의 색 변화를 Delta RGB 분석하여 나타내었다. 센서의 분해능을 높이기 위해 HRP가 접합된 goat anti rabbit IgG항체의 희석비율 및 Anti-PG와 HRP가 접합된 goat anti rabbit IgG항체의 상호 반응의 희석 비율을 최적화 하였으며 이를 통해 센서에서 항원과 항체의 면역반응을 최적화 하였다. 제작된 센서를 사용하여 PG를 검출한 결과 측정한 가능한 PG의 최소 농도는 0.25 μg 이며 PG의 측정 가능 범위는 0.25 μg-2 μg 이었다. 위 실험결과를 바탕으로 제안된 종이 기반의 효소결합 면역반응 센서는 기존 방법과 비교하여 소량의 샘플을 사용하여 짧은 시간에 PG를 검출하고 분석할 수 있다는 장점이 있지만 분해능이 낮다는 단점을 가짐을 알 수 있다. 그러므로, 제안된 PG를 검출하기 위한 종이 기반의 효소결합 면역반응 센서는 앞으로 분해능 개선된다면 농작물의 질병 유무를 판단하는데 사용될 것으로 예상되며 농작물의 생산성 향상에 기여할 것으로 기대된다.
Acknowledgments
이 연구는 2021년도 광주대학교 대학 연구비의 지원을 받아 수행되었다.
REFERENCES
-
J. D. Walton, “Deconstructing the cell wall”, Plant Physiol., Vol. 104, No. 4, pp. 1113-1118, 1994.
[https://doi.org/10.1104/pp.104.4.1113]

-
R. D´ovidio, B. Mattei, S. Roberti, D. Bellincampi, “Polygalacturonases, polygalacturonase-inhibiting proteins and pectic oligomers in plant-pathogen interactions”, Biochim. Biophys. Acta, Vol. 1696, No. 2, pp. 237-244, 2004.
[https://doi.org/10.1016/j.bbapap.2003.08.012]

-
D. F. Bateman and H. G. Basham, “Degradation of plant cell walls and membranes by microbial enzymes”, Encycl. Plant Physiol., Vol. 4, pp. 316-355, 1976.
[https://doi.org/10.1007/978-3-642-66279-9_13]

- M. Li, Z. Gao, M. Hu, S. Zhou, D. Yang, B. Yang, J. Yi, and F. Z. Yang, “Pathogenicity of cell wall degrading enzymes produced by botryodiplodia theobromae Pat. Against mangoes”, Agricultural Biotechnology, Vol. 1, No. 6, pp. 18-21, 2012.
- Y. Q. Zhao, Y. H. Wu, Y. Fu, X. X. Zhao, and J. G. Chen, “Activity pathogenic effect of cell wall degrading enzyme in tobacco target spot pathogen Rhizoctonia solani”, Tobacco Science & Technology, Vol. 11, pp. 84-88, 2014.
-
J. Zhang, B. D. Bruton, and C. L. Biles, “Cell wall-degrading enzymes of didymella bryoniae in relation to fungal growth and virulence in cantaloupe fruit”, Eur. J. Plant Pathol., Vol. 139, No. 4, pp. 749-761, 2014.
[https://doi.org/10.1007/s10658-014-0429-2]

-
A. K. Chaurasia, S. Chaurasia, S. Chaurasia, and S. Chaurasia, “In vitro and in vivo production of polygalacturonase, polymethylgalacturonase and cellulase enzymes by Alternaria solani at different incubation periods”, Afr. J. Plant Sci., Vol. 8, No. 5, pp. 248-253, 2014.
[https://doi.org/10.5897/AJPS2013.1114]

-
D. B. Gawade, R. R. Perance, A. P. Suryawanshi, C. D. Deokar, “Extracellular enzymes activity determining the virulence of rhizoctonia bataticola, causing root rot in soybean”, Physiol. Mol. Plant Pathol., Vol. 100, pp. 49-56, 2017.
[https://doi.org/10.1016/j.pmpp.2017.06.003]

-
T. Tu, K. Meng, Y. Bai, P. Shi, H. Luo, Y. Wang, P. Yang, Y. Zhang, W. Zhang, and B. Yao, “High-yield production of a low-temperature-active polygalacturonase for papaya juice clarification”, Food Chem., Vol. 141, No. 3, pp. 2974-2981, 2013.
[https://doi.org/10.1016/j.foodchem.2013.05.132]

-
G. L. Miller, “Use of dinitrosalicylic acid reagent for determination of reducing sugar”, Anal. Chem., Vol. 31, No. 3, pp. 426-428, 1959.
[https://doi.org/10.1021/ac60147a030]

-
M. Somogyi, “A new reagent for the determination of sugars”, J. Biol. Chem., Vol. 160, No. 1, pp. 61-68, 1945.
[https://doi.org/10.1016/S0021-9258(18)43097-9]

-
S. Torres, J. E. Sayago, R. M. Ordoñez, and M. I. Isla, “A colorimetric method to quantify endo-polygalacturonase activity”, Enzyme Microb. Technol., Vo. 48, No. 2, pp. 123-128, 2011.
[https://doi.org/10.1016/j.enzmictec.2010.04.004]